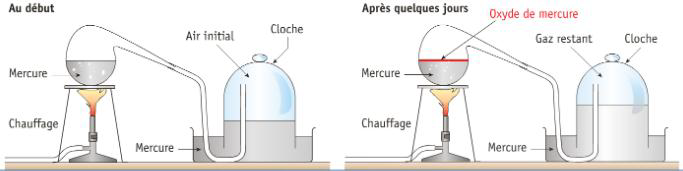
Lavoisier chauffe fortement pendant plusieurs jours du mercure dans une cornue. Il recueille de loxyde rouge à la surface du mercure et constate que le volume dair de la cloche (à droite sur le dessin) a diminué de 0,14 litre. Le gaz restant dans la cloche ne permet plus la combustion dune bougie et fait mourir une souris. Il lappelle «azote » ce qui signifie « sans vie ». Ce gaz prendra ensuite le nom de diazote.
Dans un deuxième temps, il place loxyde de mercure dans une autre cornue et le chauffe : il récupère ainsi du mercure et 0,14 litre dun gaz , »lair vital », qui stimule la flamme dune bougie et permet la respiration de la souris. Lavoisier renomme l'«air vital » en oxygène en 1777 à partir de la racine grecque oxys (acide, littéralement "âpre" d'après le goût des acides et gen?s (producteur, littéralement « qui engendre »). On lappellera ensuite dioxygène.
En mélangeant ce nouveau gaz avec celui restant sous la cloche après la première opération, il retrouve le même volume dair quau départ, soit 0,8 litre, et constate que ce mélange de gaz se comporte comme lair : il néteint pas les lumières et ne fait pas périr les animaux.
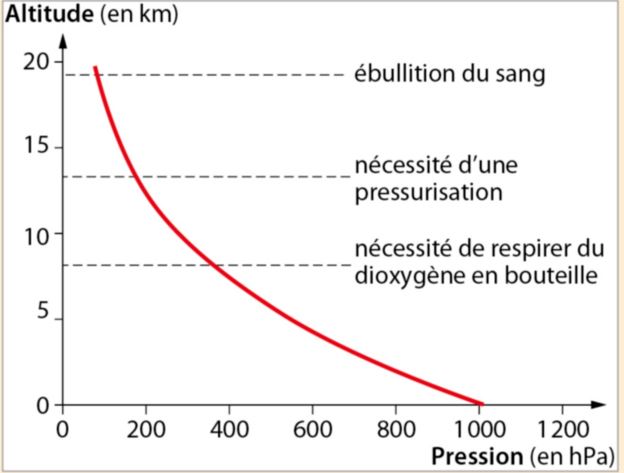
 Diagramme :
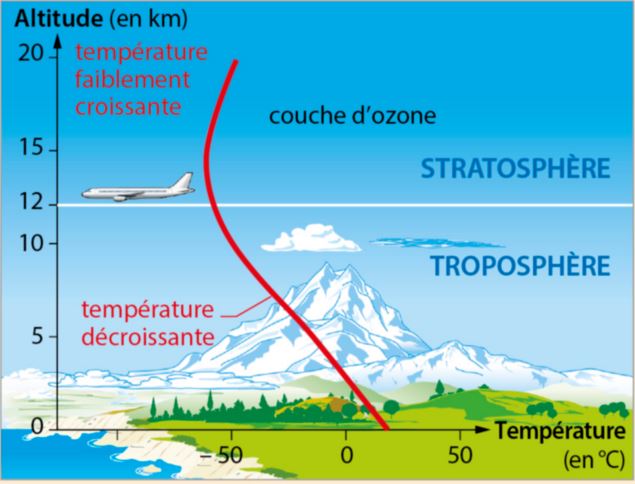
Diagramme :